武汉禾元生物科技股份有限公司品牌商
16 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 1.2000000000000002
- 0.20000000000000018
纤维连接蛋白(FN)(纤连蛋白)(外涂型化妆品原料)
询价
品牌商
武汉禾元生物科技股份有限公司
入驻年限:16 年
- 联系人:
卫经理
- 所在地区:
湖北 武汉市
- 业务范围:
技术服务、体外诊断、医疗器械、试剂、细胞库 / 细胞培养、原辅料包材
- 经营模式:
生产厂商 科研机构
推荐产品
公司新闻/正文
“类器官的肥料”——细胞因子
1095 人阅读发布时间:2023-11-06 10:59
一、类器官简介
类器官是一类基于干细胞在体外进行3D培养而形成的具有一定组织结构和功能的微型组织或器官类似物。类器官拥有与来源组织器官高度相似的组织学特征,并能一定程度上拥有该组织器官相似的生理功能。
随着 3D 细胞培养技术的兴起,以3D细胞培养技术为基础的类器官培养技术开始成为研究热点。根据新思界产业研究中心发布的《2021-2025年全球类器官行业深度市场调研及重点区域研究报告》显示,2020年,全球类器官市场规模在5亿美元左右,随着医疗技术进步,类器官市场规模将进一步扩张,预计2021-2026年,全球类器官市场规模将保持以18.2%的年均复合增长率增长。在国家多项政策的支持下,类器官的发展也进入了“快速通道”。
表1类器官相关的支持性政策
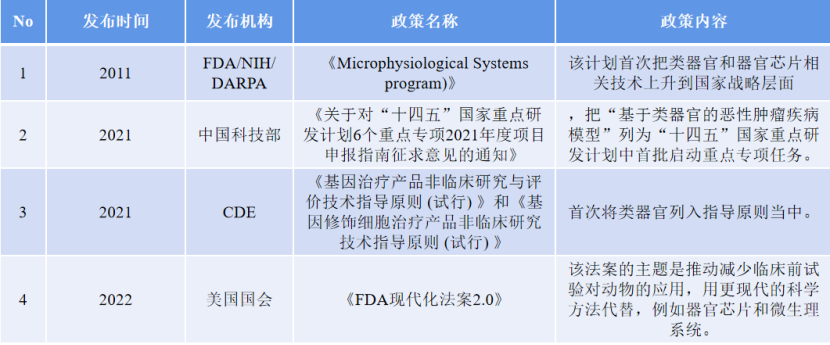
表2 国内施行的类器官相关团体标准
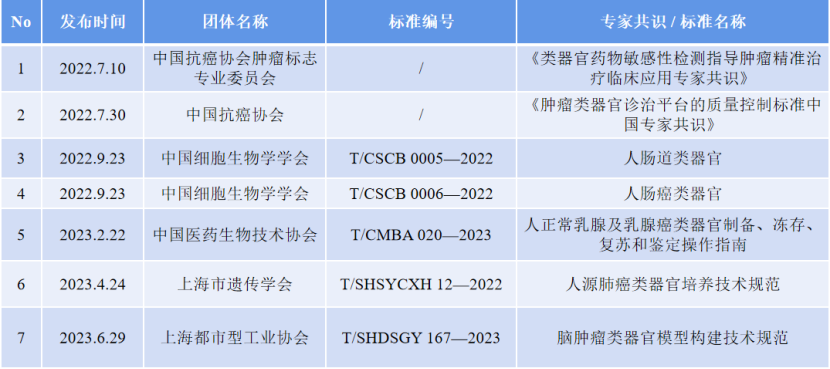
DROST团队[1]曾将2D细胞和类器官模型进行了对比,发现类器官不仅能高度模拟体内细胞生长环境,保持细胞生长的空间结构,而且能更好地代表来源组织器官的生理功能和生物学特性。目前,类器官已成功应用于病原微生物致病模型构建[2]、肿瘤研究[3]、临床药物筛选[4]、药物研发等多个领域[5],此外,新兴的单细胞测序技术[6]、CRISPR-Cas9 基因编辑技术更是为类器官研究提供了进一步发展的空间[4]。
但类器官培养并不如普通 2D 细胞培养简便,其构建成功率不仅与组织来源种类、来源组织质量、细胞生长阶段等多种因素有关,还会遇到培养基成分复杂培养条件较难优化的挑战。随着近年来各领域对类器官培养的重视,多种组织器官来源的类器官模型均有报道,但仍有某些类器官建模成功率低、培养条件不够稳定等问题存在,特别是在低分化肿瘤组织来源的类器官培养中,其成功率明显低于高分化肿瘤来源组织或正常组织,因此对已有类器官培养基相关成分进行了解和剖析就显得尤为重要,本文将重点对在类器官培养基中起到部分关键调控,如同培养类器官的“沃土”中的“肥料”——细胞因子进行介绍。
二、类器官培养的“肥料”——细胞因子
成功建立类器官的关键,除了所需的生物材料基质外,生长因子作为细胞培养、增殖及分化所必需的物质也必当优先考虑,从而保证类器官中的干细胞长期生存的能力。通过优化培养物生长条件模拟生理组织自我更新或损伤修复过程中的干细胞巢环境,如提供基底膜基质(即Matrigengel)并添加一系列激动剂(如Wnt和酪氨酸激酶受体)和抑制剂(如骨形态发生蛋白/转化生长因子-β)可达到上述目的。不同的生长因子组合也能诱导多能干细胞向不同的类器官细胞分化进而获得我们需要的类器官类型(图1),同时不同的细胞因子也是培养不同种类的类器官的关键物质(图2)。
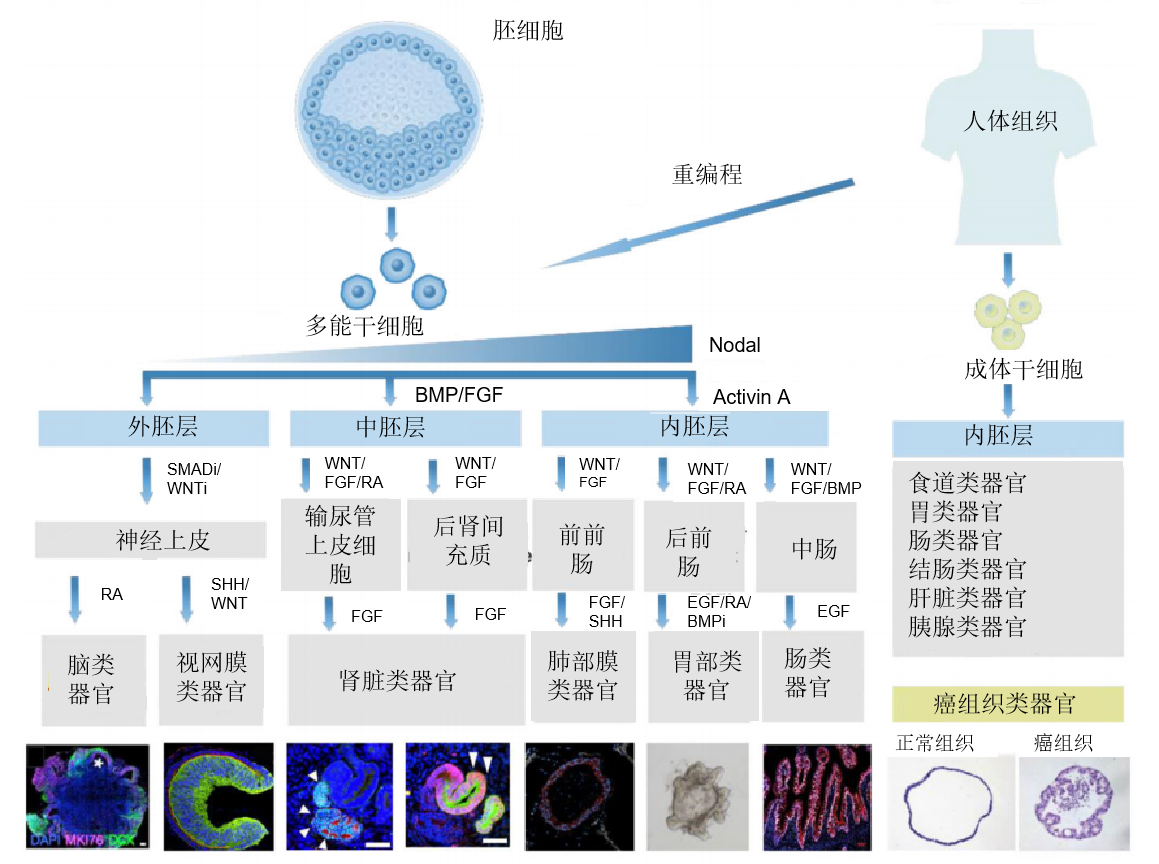
图1:生物化学型号诱导类器官形成[7]

图2 不同来源和类型的类器官对生长因子偏好性[8]。
生长因子的添加配方仍在不断改进,以进一步提高类器官体外存活率。下面将对部分生长因子进行逐一介绍。
- 表皮生长因子(epidermal growth factor,EGF):
表皮细胞生长因子是人体内一种重要的细胞因子,其功能主要是促进皮肤细胞的分裂,同时表皮细胞生长因子也可以促进细胞的增殖。在输卵管的类器官培养中,表皮细胞生长因子可以促进细胞增殖和分化[9]。此外,在小肠类器官培养中,表皮细胞生长因子可以促进肠道的生长,表皮细胞生长因子信号通路在肠类器官生长中发挥重要作用[10]。此外,表皮细胞生长因子对胶质瘤干细胞具有促进增殖的作用[11]。
- 成纤维细胞生长因子(fibroblast growth factor,FGF):
成纤维细胞生长因子广泛分布于体内多种组织器官,是一种对细胞生长、增殖以及分化具有调控作用的生长因子,其家族目前发现23个成员。成纤维细胞生长因子通过对多种信号通路发挥作用从而调控体内细胞的生长。有研究表明,成纤维细胞生长因子通过抑制骨形态发生蛋白信号以及提高 Wnt 信号传导从而在类器官培养中发挥作用[12]。而且,Sox10 可以标记乳腺类器官培养的干细胞群,成纤维细胞生长因子信号可以调节不同 Sox 家族转录因子在体内的表达以及功能[13]。在类器官培养中最常见的家族成员为成纤维细胞生长因子2(bFGF)、成纤维细胞生长因子7(KGF) 以及成纤维细胞生长因子10。成纤维细胞生长因子2 可以促进类器官的形态发生,维持胚胎干细胞的干性,也可以与胰岛素样生长因子 1 结合增强人肠干细胞的集落形成能力,促进神经干细胞的增殖、分化[14]。由此看出,成纤维细胞生长因子家族对于机体内多种细胞生长、增殖、分化具有重要的调控作用,因此也成为体外类器官培养中较常见的细胞因子之一。
- 血管内皮生长因子( vascular endothelial growth factor,VEGF):
血管内皮生长因子是一个家族,包括血管内皮生长因子 A、血管内皮生长因子 B、血管内皮生长因子 C 等多个家族成员,其主要作用为促进血管内皮细胞的生长。通常所提到的血管内皮生长因子指的是血管内皮生长因子 A,也是在类器官培养中比较常用的血管内皮生长因子,其在血管生成和内皮细胞生长中发挥作用。但在类器官培养中,其功能不再仅仅局限于血管生成等作用。研究发现,血管内皮生长因子 A 在肾脏类器官培养中可以促进小鼠后肾间充质细胞的增殖,而对于细胞的迁移没有影响[15]。在心脏类器官研究中,血管内皮生长因子信号通路通过促进Cx43 表达,以此增强心脏功能[16]。在脑类器官研究中发现,血管内皮生长因子 A 可以促进血管生成、神经分化[17]。由此看来,血管内皮生长因子促进类器官扩增、维持内环境平衡发挥重要作用。
三、植物源细胞因子
类器官行业在国内的发展势头强劲,但是仍有一些问题和阻碍亟待解决,首当其冲的就是上游耗材受到限制。细胞因子作为类器官培养的重要调控者,是类器官培养基,类器官3D打印墨水等新型产品的重要组成部分。因此类器官的培养研究,到后期的批量化扩大化的量产对相关耗材的产量与批间稳定性都提出了很高的要求。目前,类器官产品的耗材(如基质胶、维持类器官生态和分化所需的生长因子、细胞培养板等)大都处于进口垄断的状态。企业若能实现耗材的进口替代,成本有望大幅下降。而禾元生物正是将打破上游供应的国外垄断为己任,通过利用全球首创的水稻胚乳细胞生物反应器高效重组蛋白表达平台,实现规模化、批间稳定性好的产品为类器官研究提供全方位的蛋白原料解决方案,助力中国类器官产业发展走到世界最前列!
三、植物源细胞因子
类器官行业在国内的发展势头强劲,但是仍有一些问题和阻碍亟待解决,首当其冲的就是上游耗材受到限制。细胞因子作为类器官培养的重要调控者,是类器官培养基,类器官3D打印墨水等新型产品的重要组成部分。因此类器官的培养研究,到后期的批量化扩大化的量产对相关耗材的产量与批间稳定性都提出了很高的要求。目前,类器官产品的耗材(如基质胶、维持类器官生态和分化所需的生长因子、细胞培养板等)大都处于进口垄断的状态。企业若能实现耗材的进口替代,成本有望大幅下降。而禾元生物正是将打破上游供应的国外垄断为己任,通过利用全球首创的水稻胚乳细胞生物反应器高效重组蛋白表达平台,实现规模化、批间稳定性好的产品为类器官研究提供全方位的蛋白原料解决方案,助力中国类器官产业发展走到世界最前列!

参考文献
[1] Drost J, Clevers H. Organoids in cancer research. Nat Rev Cancer. 2018;18(7):407-418.
[2] Xiao S, Zhou L. Gastric Stem Cells: Physiological and Pathological Perspectives. Front Cell Dev Biol. 2020;8:571536.
[3] Frappart PO, Hofmann TG. Pancreatic Ductal Adenocarcinoma (PDAC) Organoids: The Shining Light at the End of the Tunnel for Drug Response Prediction and Personalized Medicine. Cancers (Basel). 2020;12(10):2750.
[4] Gilazieva Z, Ponomarev A, Rutland C, Rizvanov A, Solovyeva V. Promising Applications of Tumor Spheroids and Organoids for Personalized Medicine. Cancers (Basel). 2020;12(10):2727.
[4] Gilazieva Z, Ponomarev A, Rutland C, Rizvanov A, Solovyeva V. Promising Applications of Tumor Spheroids and Organoids for Personalized Medicine. Cancers (Basel). 2020;12(10):2727.
[5] Mittal R, Woo FW, Castro CS, et al. Organ-on-chip models: Implications in drug discovery and clinical applications. J Cell Physiol. 2019;234(6):8352-8380.
[6] Wei K, Korsunsky I, Marshall JL, et al. Notch signalling drives synovial fibroblast identity and arthritis pathology. Nature. 2020;582(7811):259-264.
[7] Yi SA, Zhang Y, Rathnam C, Pongkulapa T, Lee KB. Bioengineering Approaches for the Advanced Organoid Research. Adv Mater. 2021;33(45):e2007949.
[8] Tortorella I, Argentati C, Emiliani C, Martino S, Morena F. The role of physical cues in the development of stem cell-derived organoids. Eur Biophys J. 2022;51(2):105-117.
[9] Xie Y, Park ES, Xiang D, Li Z. Long-term organoid culture reveals enrichment of organoid-forming epithelial cells in the fimbrial portion of mouse fallopian tube. Stem Cell Res. 2018;32:51-60.
[10] Zhang RR, Koido M, Tadokoro T, et al. Human iPSC-Derived Posterior Gut Progenitors Are Expandable and Capable of Forming Gut and Liver Organoids. Stem Cell Reports. 2018;10(3):780-793.
[11] 米杜秋,张路阳,刘强,等. 表皮生长因子对胶质瘤干细胞增殖与侵袭的影响[J]. 解剖科学进展,2019,25(1):70-73.
[12] Boonekamp KE, Kretzschmar K, Wiener DJ, et al. Long-term expansion and differentiation of adult murine epidermal stem cells in 3D organoid cultures. Proc Natl Acad Sci U S A. 2019;116(29):14630-14638.
[13] Lu W, Kang Y. Cell lineage determinants as regulators of breast cancer metastasis. Cancer Metastasis Rev. 2016;35(4):631-644.
[14] Fujii M, Matano M, Toshimitsu K, et al. Human Intestinal Organoids Maintain Self-Renewal Capacity and Cellular Diversity in Niche-Inspired Culture Condition. Cell Stem Cell. 2018;23(6):787-793.e6.
[15] Patel M, Velagapudi C, Burns H, et al. Mouse Metanephric Mesenchymal Cell-Derived Angioblasts Undergo Vasculogenesis in Three-Dimensional Culture. Am J Pathol. 2018;188(3):768-784.
[16] Iyer RK, Odedra D, Chiu LL, Vunjak-Novakovic G, Radisic M. Vascular endothelial growth factor secretion by nonmyocytes modulates Connexin-43 levels in cardiac organoids. Tissue Eng Part A. 2012;18(17-18):1771-1783.
[17] Song L, Yuan X, Jones Z, et al. Assembly of Human Stem Cell-Derived Cortical Spheroids and Vascular Spheroids to Model 3-D Brain-like Tissues. Sci Rep. 2019;9(1):5977.